08
2023
-
05
中慧生物开发出全球首个正痘病毒广谱mRNA疫苗

2022年5月至今,猴痘病毒的全球流行引起了公众对人畜共患疾病人际传播威胁的关注1,世卫组织于2022年7月紧急宣布此次猴痘流行为国际关注的公共卫生事件。学术界和医药企业也积极提出各种防控应对策略,包括进展较快的疫苗研发。
2023年4月26日,江苏pp电子生物科技股份有限公司全资子公司易慧生物技术(上海)有限公司熊野林博士 (Vice President)和刘志华博士 (Project Director)在bioRxiv上公布了其公司关于正痘病毒广谱性mRNA疫苗的研究进展“A Quadrivalent mRNA immunization elicits potent immune responses against vaccinia and monkeypox viral antigens – a step closer to a broad orthopoxvirus vaccine” 2。

公司研发团队通过前期调研发现,除猴痘病毒外,牛痘和骆驼痘病毒在内的其他痘病毒也对人类具有传染性和一定致病性,且存在天花作为生物恐怖分子或实验室意外逃逸而再次出现的风险。
痘苗病毒、天花病毒、猴痘病毒、骆驼痘病毒、羊痘病毒和牛痘病毒的形态相近,具有一定抗原相关性3。其中参与病毒感染细胞的吸附、结合和细胞间传播的A27、A33、B5和L1及其相关同源蛋白在相关正痘病毒中高度保守,这也是上世纪痘病毒减毒活疫苗预防天花大获成功的免疫学基础4-7。抗体学研究表明,A27、A33、B5和L1存在大量广谱性中和表位8,提示这些抗原可成为广谱疫苗的候选抗原。
基于以上病原生物学与疫苗学的基础认知,团队选择将痘苗病毒表面抗原A27、A33、B5和L1 进行原创串联设计,形成单条mRNA分子,通过mRNA-LNP递送平台,开发了国际上首个针对正痘病毒属的4价广谱性mRNA候选疫苗(mRNA-ALAB)。
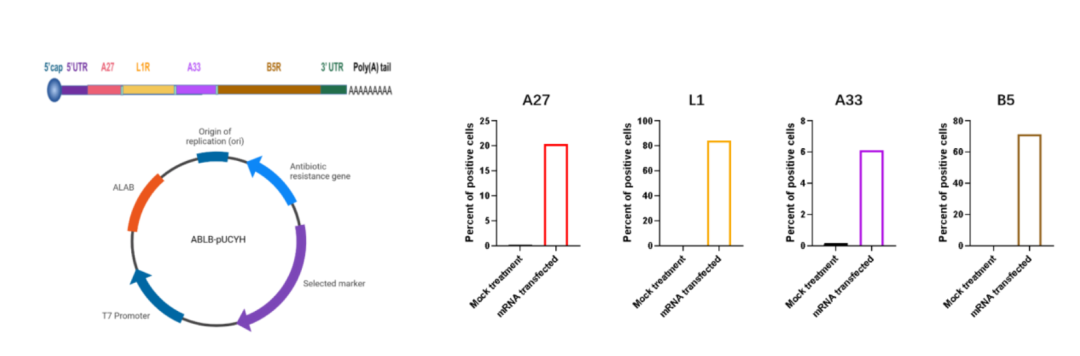
图1, mRNA-ALAB设计及体外表达验证
该4价mRNA转染HEK293T细胞,可特异性表达四个抗原分子(图1);mRNA-ALAB通过肌肉注射的方式可在小鼠体内诱导强烈的抗原特异性结合抗体和中和抗体应答(图2)、以及出色的细胞免疫应答(图3)。
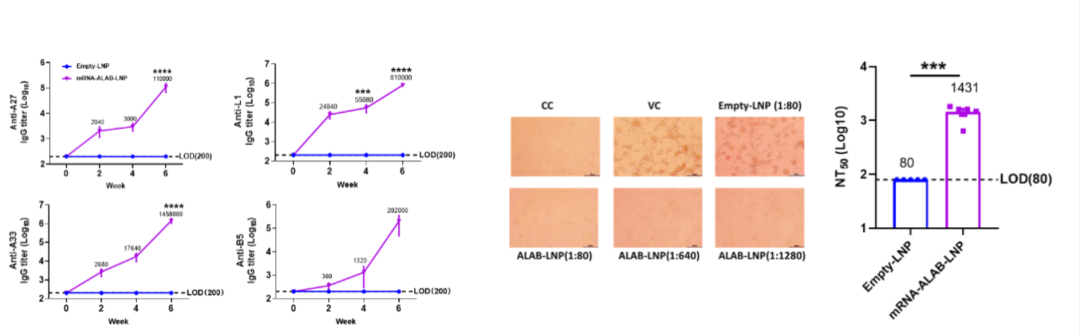
图2,mRNA-ALAB疫苗诱导的体液免疫应答
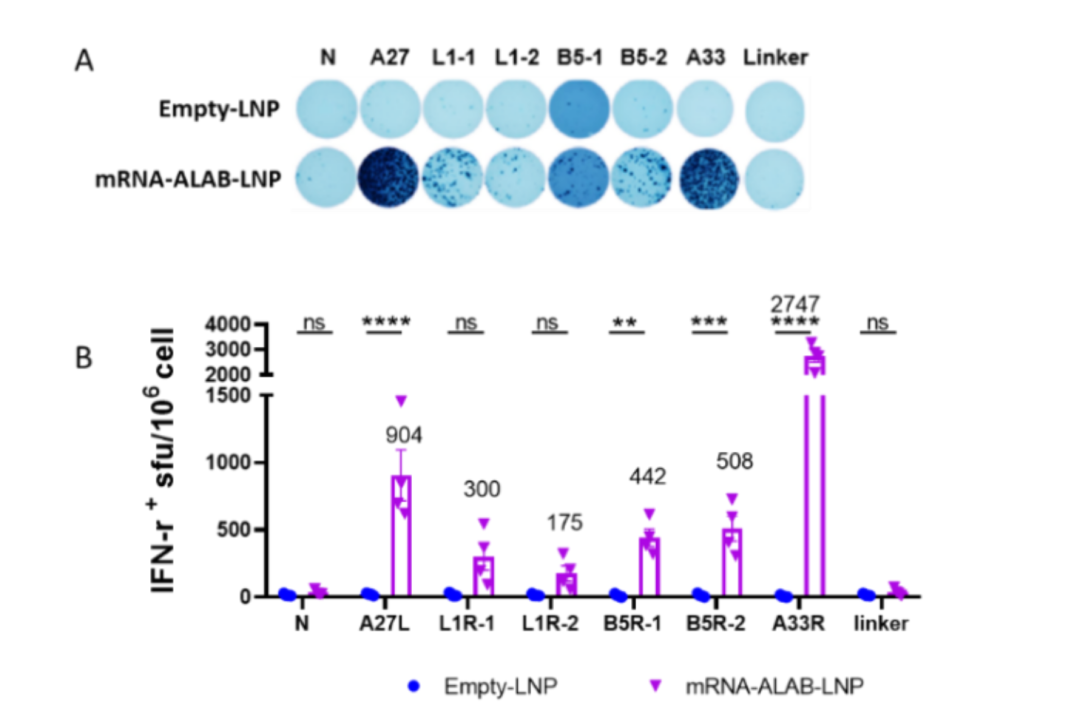
图3,mRNA-ALAB疫苗诱导的细胞免疫应答
同时该疫苗诱导的抗体可以与猴痘病毒同源抗原(A29、M1、A35和B6)发生强烈交叉结合(图4),预示该mRNA-ALAB疫苗未来可作为预防包括猴痘病毒在内的痘病毒感染的潜在候选疫苗。
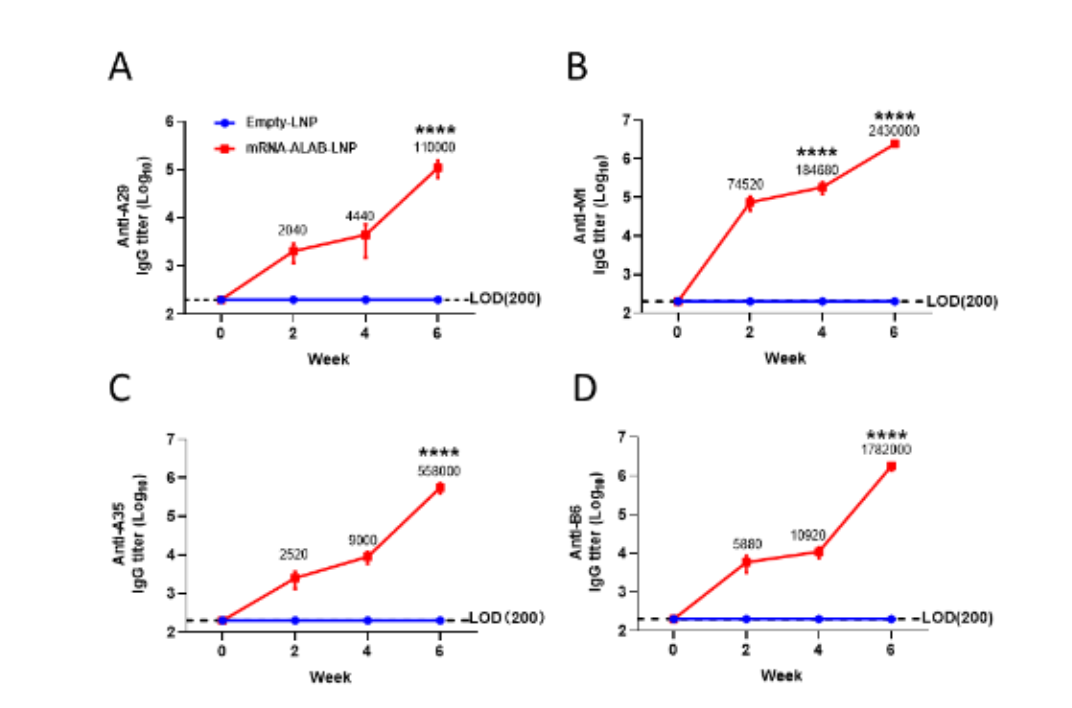
图4,mRNA-ALAB 疫苗免疫血清与猴痘抗原的交叉反应
在诱导强烈免疫反应的同时,该mRNA疫苗在动物实验中未引起任何安全性担忧,避免了由传统痘病毒减毒苗经常引起的严重副反应;在分子设计上,相较于多个mRNA分子的混合递送方式,公司开发出了单个mRNA分子递送多个抗原的原创设计,极大简化工艺过程,缩短开发周期, 具备较高的生产成本优势;为应对大规模疫情爆发,提供了一种可行的疫苗设计思路。
未来,公司研发团队还会就该疫苗的广谱性和功能性展开更多研究。
参考文献:
1. Mitjà O, Ogoina D, Titanji BK, Galvan C, Muyembe JJ, Marks M, Orkin CM. 2023. Monkeypox. Lancet 401:60-74.
2. Su C, Wen Y, Geng X, Yang C, Yin Q, Xiong Y, Liu Z. 2023. A Quadrivalent mRNA immunization elicits potent immune responses against vaccinia and monkeypox viral antigens – a step closer to a broad orthopoxvirus vaccine. bioRxiv doi:10.1101/2023.04.23.537951:2023.04.23.537951.
3. Hendrickson RC, Wang C, Hatcher EL, Lefkowitz EJ. 2010. Orthopoxvirus genome evolution: the role of gene loss. Viruses 2:1933-1967.
4. Chung CS, Hsiao JC, Chang YS, Chang W. 1998. A27L protein mediates vaccinia virus interaction with cell surface heparan sulfate. J Virol 72:1577-85.
5. Foo CH, Lou H, Whitbeck JC, Ponce-de-León M, Atanasiu D, Eisenberg RJ, Cohen GH. 2009. Vaccinia virus L1 binds to cell surfaces and blocks virus entry independently of glycosaminoglycans. Virology 385:368-82.
6. Smith GL, Vanderplasschen A, Law M. 2002. The formation and function of extracellular enveloped vaccinia virus. J Gen Virol 83:2915-2931.
7. Hooper JW, Custer DM, Thompson E. 2003. Four-gene-combination DNA vaccine protects mice against a lethal vaccinia virus challenge and elicits appropriate antibody responses in nonhuman primates. Virology 306:181-95.
8. Gilchuk I, Gilchuk P, Sapparapu G, Lampley R, Singh V, Kose N, Blum DL, Hughes LJ, Satheshkumar PS, Townsend MB, Kondas AV, Reed Z, Weiner Z, Olson VA, Hammarlund E, Raue HP, Slifka MK, Slaughter JC, Graham BS, Edwards KM, Eisenberg RJ, Cohen GH, Joyce S, Crowe JE, Jr. 2016. Cross-Neutralizing and Protective Human Antibody Specificities to Poxvirus Infections. Cell 167:684-694.e9.
更多新闻





